实验十四、单扫描极谱定性及定量分析
一、目的要求:
1.加深对极谱半波电位的意义、测量方法及应用的理解。
2.掌握直接比较法和标淮加入法两种极谱定量分析方法。
3.了解单扫描极谱法的原理及特点,初步掌握LK-98型电化学分析系统的使用方法。
二、基本原理
单扫描极谱的原理,与经典极谱相似,是根据电流-电压曲线来进行分析的。不同的是加到电解池两电极的电压扫描速度不同。经典极谱要获得一个极谱波,需要用近百滴汞,所加直流电压的扫描速度缓慢,一般为0.2v/min,单扫描极谱则是在一滴汞的形成后期的一段很短的时间內进行快速线性扫描,如JP-2型示波极谱仪控制汞滴下落时间为7s,前5s不扫描,在汞滴寿命的最后2s内扫描0.5v电压。並记录i~-Φde曲线。这样可达到汞滴定时,扫描同步,使每滴汞的i~-Φde曲线有良好的重现性。
下图为单扫描极谱仪的基本电路。V为极化电压(锯齿波电压)发生器。由它产生的扫描电压,通过R加在电解池的两极上(滴汞电极DME和对电极Pt)。电解过程中产生的电流变化,通过电阻R后产生的电压降变化,经放大后将其输入至示波器的垂直偏向板上,因此垂直偏向板代表电流座标。而工作电极与参比电极(SCE)之间的电位差经放大后输入示波器的水平偏向板上,因此水平偏向板代表工作电极的极化电压。于是,示波器的荧光屏上将出现完整的极化曲线。这种三电极系统可使工作电极的电位变化速度恒定而不受电路中iR电位降的影响。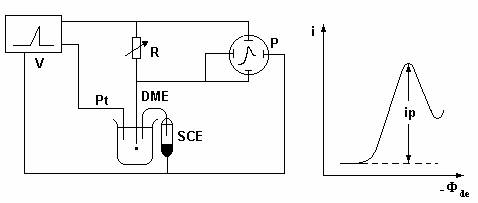
由于单扫描极谱的电压扫描速度非常快,当达到可还原物质的分解电压时,该物质在电极上迅速还原,产生很大的电流。由于可还原物质在电极附近浓度迅速降低,而溶液主体中的可还原物质又来不及扩散到电极,因此电流迅速下降,直至电极反应速度和扩散速度达到平衡。这样就在极谱曲线上出现尖峰状。
由于电极反应速度快,峰电流比经典极谱测得的扩散电流要大得多,因而灵敏度要高1-2个数量级。而且测量峰高比测量波高分辨率高、精密度高。对于可逆性差或不可逆电极反应,由于电极反应速度跟不上电压扫描速度,所得图形的尖峰状就不明显甚至没有尖峰。
对于可逆电极反应,峰电流方程式可如下表示:
ip = 2.69×105 n3/2 D1/2 v1/2 A c
式中,A为电极面积(cm2);v为电压扫描速度(v/s),其他与尤考维奇方程式相同。 所以,在一定的底液及实验条件下,峰电流与被测物质的浓度成正比。这是单扫描极谱定量分析的依据。
峰电位与半波电位的关系是:
还原波: Φp=Φ1/2 - 1.1 RT/nF =Φ1/2 – 0.028/n (25℃)
氧化波: Φp=Φ1/2 +1.1 RT/nF =Φ1/2 + 0.028/n (25℃)
由于q = c v (q-双电层电荷;c-电容;v-电压)所以电容电流ic=dq/dt=vdc/dt+cdv/dt,其中,dc/dt ∝dA/dt。在经典极谱中,dv/dt很小,dA/dt较大;而在单扫描极谱中,
dA/dt很小,dv/dt较大, 故两者均无法克服电容电流的影响。
三、仪器和试剂
1.JP-2型示波极谱仪;LK-98A型电化学分析系统;
25ml烧杯3只、 吸量管: 10ml 1支、 2ml 6支。
2.浓度各为1mg/ml的Cu2+、Cd2+、Ni2+、Zn2+标准溶液;
0.5%明胶; 2mol/L NH3-NH4Cl; 10%Na2SO3; 未知试液。
四、操作步骤
1.在25ml比色管①中,加1mg/ml的Cu2+、Cd2+、Ni2+、Zn2+标准溶液各1.0ml;2mol/L NH3-NH4Cl溶液10.0ml;10%Na2SO3溶液2.0ml; 0.5%明胶4滴; 加水至刻度后摇匀。在单扫描极谱仪上分別测定的峰电位Φp和峰电流ip。
2.在另一25ml比色管②中,加入未知液1.0ml。其余底液同上。定容摇匀后,测定
未知液中各元素的峰电位Φp和峰电流ip。并根据Φp确定未知液的组成,比较标液和未知液中相应元素的ip用直接比较法对未知液定量(记下未知液号码)。
3.未知液中选一元素A用标准加入法测其浓度。根据CsVs≈(1/2~1)CxVx计算应加入的标液量VsA。
4.在比色管③中,加入未知液1.0ml,加入A标液VsAml,加入同量底液后测定峰电流,和比色管②中该元素峰电流相比较,用标准加入法求未知液中该元素浓度。
五、实验记录及数据处理
1. 线性扫描伏安法工作参数
|
灵敏度 |
滤波参数 |
放大倍率 |
初始电位 |
终止电位 |
扫描速度 |
汞滴生长时间 |
|
μA/V |
HZ |
|
-0.200 V |
V |
V/S |
S |
2. Cu2+、Cd2+、Ni2+、Zn2+标准溶液的Φp和ip测定(比色管①) Vs=1.0ml Cs=1.0mg/ml
|
离子 |
Cu2+(Ⅱ) |
Cd2+ |
Ni2+ |
Zn2+ |
|
|
峰电位Φp (v) |
|
|
|
|
|
|
峰电流ip (μA) |
第一次 |
|
|
|
|
|
第二次 |
|
|
|
|
|
|
平均 |
|
|
|
|
|
1. 未知液中离子的Φp和ip测定(比色管②)
未知液 # Vx=1.0 (ml)
|
离子 |
峰电位Φp (v) |
峰电流ip (μA) |
浓度 (mg·ml-1) |
||
|
第一次 |
第二次 |
平均 |
|||
|
A: |
|
|
|
|
|
|
B: |
|
|
|
|
|
2. 标准加入法(比色管③) Vx= ml VsA = ml
|
离子 |
峰电位 Φp (v) |
峰电流ip (μA) |
浓度 (mg·ml-1) |
||
|
第一次 |
第二次 |
平均 |
|||
|
A: |
|
|
|
|
|
计算公式:
CA= = mg·ml-1
六、注意事项
1.绝对不允许在插上电解池插头,电极浸在电解池中的情况下开机或关机。由于在开机或关机的一瞬间,电解池两端会出现很高的电压,使浸在电解池中的毛细管孔立即遭到破坏。只能在开机之后,才能放心地将电极浸入电解池。
2. 实验完毕,先取下电解池,沖洗电极,用滤纸拭干,放下贮汞瓶,然后关电源。
3. 注意汞的安全使用,用过的含汞试液切不可直接倒入水槽;毛细管下始终放置有水的烧杯;注意不要让汞洒落在桌上或地上。一旦洒落,要尽量收集起来。实在不能收集的,再覆盖硫磺处理。
七、问题讨论
1.和经典极谱相比,单扫描极谱有什么优点?为什么?能否用增大极化电压的扫描速度再继续提高它的灵敏度。
2.单扫描极谱何以可省去除氧操作?
附录 某些金属离子的半波电位(v)VS·SCE
|
金属离子 |
1mol/LKCl |
1mol/LHCl |
1mol/LKOH (NaOH) |
2mol/LHAC+ 2mol/LNaAC |
1mol/LNH3+ 1mol/LNH4Cl |
|
|
Cu2+ |
Ⅰ |
+0.04 |
+0.04 |
-0.41 |
-0.07 |
-0.24 |
|
Ⅱ |
-0.22 |
-0.22 |
-0.51 |
|||
|
Cd2+ |
-0.64 |
-0.64 |
-0.76 |
-0.65 |
-0.81 |
|
|
Ni2+ |
-1.10 |
— |
— |
-1.10 |
-1.10 |
|
|
Zn2+ |
-1.00 |
— |
-1.48 |
-1.10 |
-1.35 |
|