实验十三、库仑滴定法测定砷
一、 实验目的
1.学习和掌握库仑滴定法的基本原理;
2.练习简易库仑滴定仪的安装、使用和滴定操作;
3.测定试液中痕量砷的含量。
二、基本原理
库仑滴定法是建立在控制电流电解过程基础上的一种相当准确而灵敏的分析方法,可用于微量分析及痕量物质的测定。它是在恒电流条件下,以100%的电解效率,电解某一溶液,使产生一种能与被测物质进行定量化学反应的物质(滴 定剂)。因为一定量的被分析物质需要一定量的“滴定剂”与之作用,而此一定 量的“滴定剂”又是被一定量的电量所电解出来的。故由电解所消耗的电量即可按法拉第定律求得被分析物质含量。这种滴定方法所需滴定剂不是由滴定管加入的,而是借助于电解方法产生的。滴定剂的量与电解所消耗的电量成正比。所以称为“库仑滴定”。库仑滴定反应的终点可以用指示剂,电位法或电流法来指示。影响测定精度的主要因素是终点确定、电量的精确测定和电流效率必须为 100%,即通过电解池的电流全部用于电解被测定的物质。
本实验是用恒电流电解碘化钾缓冲液(用碳酸氢钠控制溶液pH值)。在阳极上碘离子氧化为碘,生成的碘立即与溶液中的As(Ⅲ)作用:
2I- —2e=I2
I2+AsO33-+H2O=2I-+AsO43-+2H+
分别用淀粉指示剂或“死停法”确定终点。当砷(Ⅲ)全部被氧化为砷(Ⅴ) 后,过量的砷将淀粉溶液变为兰紫色,指示终点达到。当用死停法指示终点时,此时指示系统中检流计光点突然发生移动,即为终点到达。根据测量电解时所消耗的电流值和时间,即可按法拉第定律计算溶液中砷的含量。
W=i·t·M/96487·n
其中: M—待测物分子量(或原子量)(As 74.922); i—电解电流;
n—电极反应电子数; t—电解时间。
为了保证100%电流效率,在试液中加入大量KI。电解对其浓度影响很小, 因而不需在电解过程中增加电解电压,从而避免了在直接由恒电流电解被测离子情况下,待测离子减低而需增加电解电压而引起的副反应。此外,在电解池中采用大面积铂片电极,加强搅拌等措施避免浓差极化产生。
三、仪器和试剂
(一)仪器
1. 本实验采用单元仪表组合的简易库仑滴定装置(如图5—1所示)。
R1、R4—可变电阻 R2—50Ω标准电阻 R3—500Ω电阻
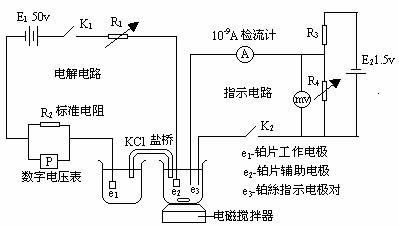
图5—1 简易库仑滴定装置图
2. 电磁搅拌器及搅拌磁子 1台 3. 秒表 1只 4. 量筒、吸量管
5. KLT-1型通用库伦仪
(二)试剂
1. 碘化钾缓冲溶液:
溶解120克KI、20克碳酸氢钠,稀释至1升,加入亚砷酸溶液2—3毫升,以防止被空气氧化。
2. 0.5mol·L-1 Na2SO4 3. 0.5%淀粉溶液(新配制)
4. 1:1硝酸 5.亚砷酸未知液
100μg/mLAs(Ⅲ)溶液配制:
准确称取三氧化二砷0.1320克,放置于100mL烧杯中,加5 mL20%NaOH,温热至三氧化二砷全部溶解后,以酚酞作指示剂,用1 mol·L-1H2SO4中和至无色,再过量10 mL,转入1升容量瓶中用蒸馏水稀释至刻度。
四、实验步骤
(一) 指示剂法确定终点
1、按图5—1连接线路,安装成简易的库仑滴定仪。铂电极需浸于温热的1:1硝酸中数分钟,取出后用水洗净,用滤纸吸干水份。
2、电解池阳极区
取一个50 mL烧杯,加入25 mL0.5 mol·L-1Na2SO4溶液,2 mL 1mol·L-1 KI溶液及淀粉溶液20滴,放入搅拌磁子,置于电磁搅拌器上,作阳极区。
3、电解池阴极区
另取一个50 mL烧杯,加入30 mL0.5 mol·L-1 Na2SO4溶液,作阴极区。
4. 将铂片电极或铂网电极分别浸入阳极区和阴极区的溶液中,用盐桥将阳极区和阴极区连接起来,启动电磁搅拌器。
5. 合上电键K1,调节转盘电阻箱R1,使电解电流为2毫安(设定标准电阻R2为50Ω,调节到数字电压表P示值为100mV)。同时进行预电解, 直至阳极区的溶液刚出现兰紫色而不褪去时,拉开电键K1,停止预电解。
6. 准确吸取2.00毫升亚砷酸未知液于阳极区的烧杯中,再合上电键,同时按动秒表开始计时。注意随时调节R1,使保持恒电流为2.00毫安。 当电解至溶液刚出现兰紫色而不褪去时,按下秒表停止计时,打开电键K1。
7. 记录电解时间和电压表上读数,计算电解电流,最后计算亚砷酸浓度。
8. 另取试液更换阳极区溶液,作重复实验共三次,求得亚砷酸浓度的平均
(二) 电流法——“死停法”确定终点(KLT-1型通用库伦仪)
1.在电解池中加入70ml 0.5mol/LNa2SO4溶液(约电解池体积的一半),5ml 1mol/LKI溶液,放入搅拌子。在电解阴极管中加入适量0.5mol/LNa2SO4溶液,使其浸没铂丝电极。
2.连接电解电极、指示电极线。打开仪器电源,按下“电流”“上升”键。
3. 准确吸取2ml亚砷酸未知液,从电解池侧面加液口加入,将电解池置于电磁搅拌器上搅拌。(注意:搅拌速度从小到大调节,避免搅拌子碰到电解池内玻璃管和电极)
4.将仪器上“极化电位”钟表电位器预先调至0.4左右,极化电流量程调至5mA,按下“启动”琴键,按下“极化电位”键,调节“极化电位”钟表电位器至200mV(即50μA表头指示至20左右),松开“极化电位”键,待表头指针稍稳定,按一下电解电钮,指示灯灭,“工作、停止”开关置工作位置,开始电解计数,电解至终点时表头指针开始向右面突变。红灯亮,仪器读数即为总消耗的电量毫库仑数(mQ)。立即将“工作、停止”开关置“停止”位置,记录读数。
5.每次电解滴定至终点后,弹出“启动”琴键,仪器自动清零。再向滴定池内加入2ml亚砷酸未知液,重复3,4步骤的操作。平行测定3次。
五、结果处理
分别计算三次测得砷试液浓度As(μg/mL),求其平均值。
六、注意事项
1. 电解电流测定要求准确。本处采用I=毫伏数/标准电阻计算的。若电流表已作过校正,也可直接使用。随着电解的进行,电流有微小变化,这时应随时调节R1,使电流保持恒定。
2. 用指示剂法测定终点时,预电解终点溶液颜色和正式测定时终点颜色应一致。
七、问题讨论
1. 写出两个电极上的电极反应式及库仑滴定的反应式。
2. 本实验的电解电路是怎样获得恒电流的?
3. 讨论本实验滴定中可能的误差来源及其预防措施。
4. 为什么在加入未知浓度的砷试液前,先要进行预电解,使阳极区溶液刚出现不褪的兰紫色为止。