一、本章学习要求、重点和难点
1、 本章学习要求
1)掌握化学计量点、指示剂、滴定终点、滴定剂、标准溶液及滴定误差等概念;
2)了解滴定分析的过程和方法特点,掌握滴定反应的条件;
3)理解四种滴定方式(直接滴定、返滴定、转换滴定和间接滴定);
4)掌握物质量浓度和滴定度的概念、计算方法及相互间关系;
5)掌握标准溶液配制方法;
6)了解标准溶液标定中常用的基本基准试剂及对基准试剂的要求;
7)掌握四大滴定中有关反应的计量关系及浓度或含量的基本计算方法。
2、 本章学习重点
1)化学化学计量点、指示剂、滴定终点、滴定误差、滴定度、基准试剂等概念;
2)标准溶液的配制方法;
3)满足滴定反应的要求;
3)有关浓度或含量的基本计算方法。
3、 本章学习难点
1)滴定度概念,物质量浓度与滴定度相互关系
二、基本术语和概念
1、滴定分析法(容量分析法):使用滴定管将一种已知准确浓度的试剂溶液即标准溶液,滴加到待测物的溶液中,直到待测组分恰好完全反应(化学计量点),根据标准溶液浓度和所消耗的体积,计算出待测组分的含量,这类分析方法称为滴定分析法。又称“容量分析法”。
2、化学计量点(stoichiometric point):滴加的标准溶液与待测组分恰好反应完全的这一点,称为化学计量点。
3、滴定终点(end point):在滴定过程中,指示剂正好发生颜色变化的转变点,称滴定终点。
4、终点误差(end point error):滴定终点与等当点不一定恰好符合,由此造成的分析误差,称为终点误差。
5、用于滴定分析的化学反应需满足的条件
1)化学反应有确定的化学计量关系;
2)化学反应应没有副反应且定量进行;
3)反应速度较快;
4)有合适的方法确定终点。
6、滴定方式
1)直接滴法:如滴定反应符合滴定分析的要求,就可用标准溶液直接滴定被测物质。如强酸碱间的滴定。
2)返滴定法:若滴定反应速度较慢或没有合适指示剂,可先加入过量的滴定剂,待反应完全后,再用另一种标准溶液滴定剩余滴定剂,由反应所消耗滴定剂的量,就可计算出被滴定组分含量。如配位滴定法测铝含量。
3)置换滴定法:对不按一定反应式进行或伴有副反应的反应,不能采用直接滴定法。这时,可加适当试剂使之与被测物质起反应,然后滴定反应的产物,由滴定剂消耗量,产物和被测物的计量关系,计算被测物质的含量。如用K2Cr2O7滴定Na2S2O3。
4)间接滴定法:对不能与滴定剂直接反应的物质,可以通过另外的反应间接进行滴定。如氧还反应滴定钙。
7、基准物应具备的条件
1)必须具有足够的纯度;(>99.9%)
2)组成与化学式完全相同;
3)稳定;
4)具有较大的摩尔质量,
8、标准物质配制方法
1)直接配制法:直接用容量瓶配制,定容。
可直接配制标准溶液的物质应具备的条件:
(1)必须具备有足够的纯度。一般使用基准试剂或优级纯;
(2)物质的组成应与化学式完全相等,应避免结晶水丢失和潮解;
(3)稳定——见光不分解,不氧化, 不吸收空气中CO2
2)间接配制(步骤)
(1) 配制溶液:配制成近似于所需浓度的溶液。
(2)标定:用基准物或另一种已知浓度的标准溶液来滴定。
(3)确定浓度:由基准物质量(或体积、浓度),计算确定之。
9、滴定度:滴定度指每mL标准溶液相当于被测组分的质量。表示为(T滴定剂/被测物)。单位为 g/mL
三、基本公式和运算
1、物质量浓度
物质B的物质的量用 nB 表示,是国际单位制中七个基本量之一,与物质的质量 mB 是相互独立的量。设MB是物质B的摩尔质量,其关系为:
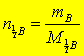
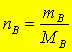 或:
或:
物质B的物质的量浓度或简称浓度CB,其定义为:
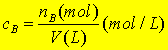 |
2、滴定度与物质量浓度的关系
滴定度指每mL标准溶液相当于被测组分的质量。表示为(T滴定剂 /被测物)。单位为 g/mL
如1.00mLHCl溶液刚好能中和0.0040gNaOH,则盐酸的滴定度可用下式表示:
T HCl/NaOH = 0.0040g/mL
1mLKMnO4标准溶液能把0.005682gFe2+氧化成Fe3+。表示为:
T KMnO4 /Fe= 0.005682g/mL
对任一滴定反应:aA + bB = cC + dD
A为被测组分,B为标准溶液,若以VB为反应完成时标准溶液消耗的体积(mL),根据反应时的摩尔关系有:
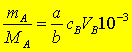 |
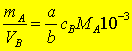 |
||
3. 分析结果的表示方法
1)待测组分的化学表示形式。分析结果通常以待测组分实际存在形式的含量表示;待测组分的实际存在形式不清楚,则分析结果最好以氧化物或元素形式的含量表示;在工业分析中,有时还用所需要的组分的含量表示分析结果;电解质溶液的分析结果,常以所存在的离子的含量表示。
2)待测组分含量的表示方法:
① 固体试样:固体试样中待测组分的含量,通常以质量分数![]() 表示。它表示试样中含待测物质B的质量mB与试样的质量mS之比,即
表示。它表示试样中含待测物质B的质量mB与试样的质量mS之比,即
![]()
或试样的B百分含量 ![]()
当待测组分含量非常低时,可采用![]() g·g -1(10 -6),ng·g -1(10 -9),pg·g -1(10 -12)表示。
g·g -1(10 -6),ng·g -1(10 -9),pg·g -1(10 -12)表示。
② 液体试样:液体试样中待测组分含量的表示方法有以下几种:
a. 物质的量浓度:待测组分的物质的量除以试液的体积,单位为mol·L-1。
b. 质量摩尔浓度:待测组分的物质的量除以试液的质量,单位为mol·kg -1。
c. 质量分数:待测组分的质量除以试液的质量,量纲为l。
d. 体积分数:待测组分的体积除以试液的体积,量纲为l。
e. 摩尔分数:待测组分的物质的量除以试液的物质的量,量纲为l。
f. 质量浓度:单位体积中某种物质的质量,单位为:mg·L-1,![]() g·L-1,
g·L-1,![]() g·mL-1,ng·mL-1,pg·mL-1。
g·mL-1,ng·mL-1,pg·mL-1。