实验八 碘和硫代硫酸钠溶液的配制与标定
实验九 葡萄糖含量的测定
一、实验目的
1、掌握Na2S2O3及I2溶液的配制和标定方法
2、掌握间接碘量法测定葡萄糖含量的方法
二、实验原理
1、硫代硫酸钠的标定
Na2S2O3不稳定,见光、受热、酸性溶液中易分解,易被氧化,需间接配制
Na2S2O3标定是采用间接碘量法。准确称取一定量的K2Cr2O7 基准试剂,配成溶液,加入过量的KI,在酸性溶液中定量地完成下列反应:
![]()
![]()
生成的I2,立即用Na2S2O3溶液滴定。![]()
有关系:![]() ,根据滴定Na2S2O3消耗的体积,即可计算出Na2S2O3的浓度。
,根据滴定Na2S2O3消耗的体积,即可计算出Na2S2O3的浓度。
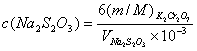
2、I2溶液的标定(略)
由式:![]() 相互滴定,可计算出I2的浓度。
相互滴定,可计算出I2的浓度。
3、葡萄糖溶液的测定
碘与NaOH作用能生成NaIO,而C6H12O6能定量地被NaIO氧化。在酸性条件下,未与C6H12O6作用的NaIO可转变为I2析出,只要用标准Na2S2O3溶液滴定析出的I2,便可计算C6H12O6的含量。有关反应:
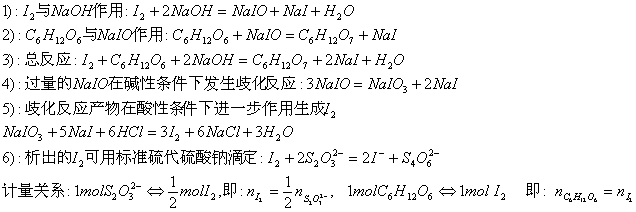
![]()
三、实验步骤
1、0.05mol/L I2和0.1mol/L Na2S2O3溶液的配制(已配好)
2、I2和Na2S2O3溶液的比较滴定
用移液管取25.00mL标准I2于锥形瓶中,加入50mL水,用Na2S2O3溶液滴定至浅黄色后,加入2mL的淀粉指示剂③,再用Na2S2O3溶液继续滴定至蓝色刚好褪去为止。平行滴定2次。
3、Na2S2O3溶液的标定
准确地称取0.11~0.12g的K2Cr2O7基准试剂2份。分别置于2个250mL的碘量瓶中,分别加入10~20mL蒸馏水使之溶解。加10mL 20% KI溶液 , 10mL 2mol/LHCl,充分混合溶解后,盖好塞子,以防止I2因挥发而损失。在暗处放置5min①,然后加50mL水稀释②,用Na2S2O3溶液滴定到溶液呈浅绿黄色时,加2mL淀粉溶液③,继续滴入Na2S2O3溶液直到蓝色刚好消失④而Cr3+绿色出现为止。
4、葡萄糖的测定
用移液管吸取25.00mL待测葡萄糖溶液于碘量瓶中,准确加入25.00mLI2 标准溶液。一边摇动,一边慢慢加入2mol/L NaOH溶液,直到溶液显淡黄色⑤。将碘量瓶加塞于暗处放置10~15min后,加2mL6mol/L HCl使溶液呈酸性,立即用Na2S2O3溶液滴定到溶液呈淡黄色,加入2mL淀粉指示剂,继续滴加到蓝色消失为止,记下读数。平行测定2次。
四、结果与计算
|
实验内容 |
数据记录 |
1 |
2 |
平均 |
|
Na2S2O3溶液的标定 |
M(K2Cr2O7)(g) |
|
|
|
|
V(Na2S2O3)(mL) |
|
|
|
|
|
C(Na2S2O3)(mol/L) |
|
|
|
|
|
I2溶液的标定 |
V(I2)(mL) |
|
|
|
|
V(Na2S2O3)(mL) |
|
|
|
|
|
C(I2)(mol/L) |
|
|
|
|
|
葡萄糖含量的测定 |
V(C6H12O6)(mL) |
|
|
|
|
V(Na2S2O3)(mL) |
|
|
|
|
|
%( C6H12O6) |
|
|
|
C6H12O6的分子量为:180
五、注意事项
1、K2Cr2O7与I2的反应不是立即完成,在稀溶液中进行更慢,所以一般需要放置5min以上。
2、K2Cr2O7还原后生成的Cr3+呈绿色,妨碍终点指示剂观察,需加水稀释,使颜色变浅。稀释还可降低过量I-,避免空气中的O2氧化。
3、Na2S2O3滴定I2时,淀粉不宜过早加入,否则易与大量I2形成加合物,加合物中的I2不易与Na2S2O3作用。
4、滴定到终点的溶液,经一段时间后变蓝。如果不是很快变蓝,那是因空气中的氧化作用所致。如果很快变蓝,而且不断加深,说明溶液稀释太早,K2Cr2O7和KI的反应在滴定前进行得不完全,此时实验失败。
5、此处,加碱的速度不宜过快,否则过量的NaIO来不及氧化C6H12O6而歧化为不与葡萄糖反应的NaIO3和NaI,使测定结果偏低,此时的颜色也需仔细地观察。
六、思考题:
1、用Na2S2O3溶液滴定I2溶液和用I2溶液滴定Na2S2O3溶液时都是用淀粉指示剂,为什么要在不同时候加入?终点颜色变化有何不同?
2、标定Na2S2O3溶液时,加入的KI溶液的量是否要很精确?为什么?